개요
의료기기법 시행규칙 제9조에 따른 의료기기 기술문서 심사 업무를 수행
주요업무
- 의료기기 기술문서 심사
- 의료기기 기술문서 변경 심사
심사 범위 및 대상 품목
1. 심사범위
해당 제품의 제조업자(수입업자)별, 품목류별 또는 품목별(모델명)별로 심사하는 것을 원칙으로 하며, 심사의뢰서를 제출받은후 추가된 제품은 심사에서 제외한다. 다만, 동일제품군에 대하여는 하나의 심사의뢰서를 제출할 수 있다.
2. 변경심사 대상
이미 허가ㆍ인증받은 제품의 허가ㆍ인증된 항목 중 허가고시 [별표4] 변경대상 판단 흐름도에 따라 안전성이나 유효성에 영향을 미치는 변경허가ㆍ인증를 받고자 하는 의료기기.
3. 심사대상 품목
의료기기 품목 및 품목별 등급에 관한 규정 별표에 의한 2등급 의료기기 중 식품의약품안전처장이 지정한 품목
4. 심사대상 제외
- 이미 허가를 받은 의료기기 구조, 원리, 성능, 사용목적 및 사용방법 등이 본질적으로 동등하지 않거나 임상시험 자료 제출이 필요한 의료기기
- 유헬스케어 의료기기에 해당하는 품목
- 소분류 품목으로 분류되지 아니하여 새로이 품목지정이 필요한 의료기기
- 의약품 또는 의약외품과 조합되거나 복합 구성된 의료기기
- 수출용 의료기기
- 동등공고제품
- 동일제품임을 확인받은 의료기기
- 경미한 변경대상 의료기기
신청서류
- 의료기기 기술문서 등 심사의뢰서 신청서 바로가기
- 의료기기 기술문서 등 심사의뢰서 작성방법 다운로드
- [별지 제3호] 본질적 동등품목 비교표 다운로드
- [별지 제2호]체외진단장비의 본질적 동등품목 비교표 다운로드
- [별지 제2호]체외진단시약의 본질적동등품목비교표 다운로드
- [별지 제13호] 의료기기 소프트웨어 적합성 확인 보고서 다운로드
- [별표 13] 의료기기 소프트웨어 적합성 확인 보고서 작성방법 다운로드
- 기술문서 변경심사 구비서류 다운로드
기술문서 심사절차 및 신청안내
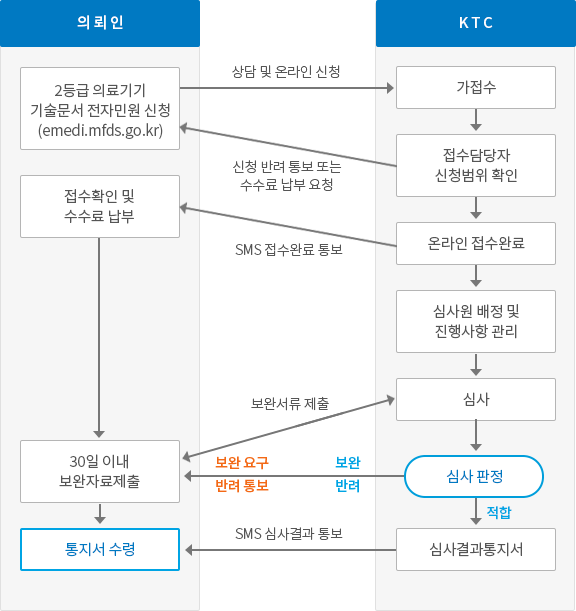
처리기한
- 기술문서 심사 : 25 일 이내
- 변경심사 : 15 일 이내 (* 공휴일 및 기술문서 보완기간은 처리기간에서 제외)
수수료(VAT별도)
관련법, 제도
- 의료기기법 제6조 (제조업의 허가 등)
- 의료기기법 제15조 (수입업의 허가 등)
- 의료기기법 시행규칙 제4조 (제조허가ㆍ제조인증ㆍ제조신고의 대상)
- 의료기기법 시행규칙 제5조 (제조허가의 절차)
- 의료기기법 시행규칙 제6조 (제조인증의 절차)
- 의료기기법 시행규칙 제9조 (기술문서 심사)
- 의료기기법 시행규칙 제26조 (허가사항의 변경허가 신청 등)
- 의료기기법 시행규치 제30조 (수입허가 신청 등)
- 의료기기 허가, 신고, 심사 등에 관한 규정
- 의료기기 품목 및 품목별 등급에 관한 규정
담당부서 홈으로 바로가기
아래버튼을 클릭하시면 담당부서의 홈으로 바로 연결되며 각 업무의 담당자 연락처를 확인하실 수 있습니다.